
La morte di una cellula può rappresentare una fonte di pericolo per l’integrità dei tessuti: per questo motivo gli organismi pluricellulari hanno sviluppato una modalità di morte cellulare che mira ad annullare possibili effetti traumatici. Tale modalità viene denominata apoptosi.
In un organismo pluricellulare la morte di una cellula può rappresentare una fonte di pericolo per l’integrità dei tessuti. Condizioni di stress fisico e chimico di particolare intensità, infatti, determinano la rottura delle membrane cellulari con conseguente rilascio del contenuto del citoplasma. La morte per necrosi è un evento pericoloso sia per il rilascio di molecole, quali enzimi proteolitici, che provocano un danno alla cellula vicina, sia perché determina una condizione pro-infiammatoria.
Un altro aspetto da considerare è il rilascio di antigeni intracellulari verso i quali l’organismo non ha sviluppato tolleranza immunitaria e che sono quindi potenziale fonte di autoimmunità.
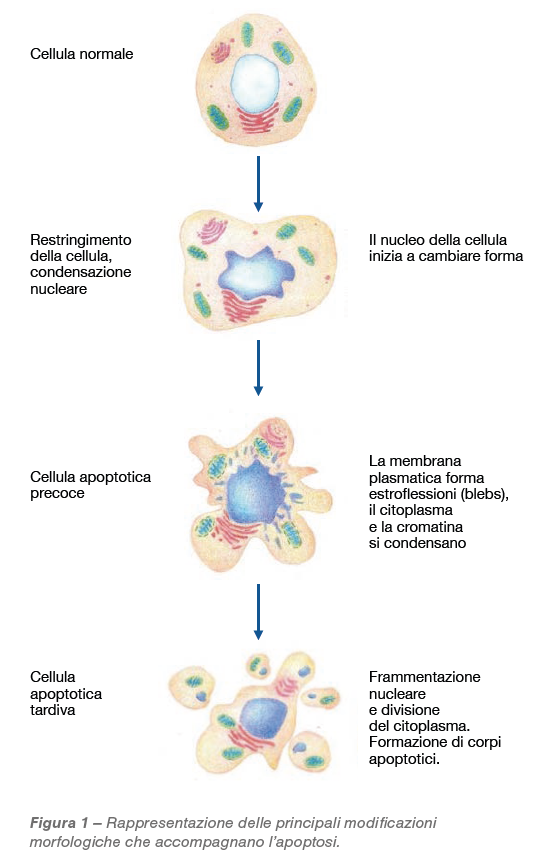
In condizioni di stress più blande o per necessità fisiologiche, gli organismi pluricellulari hanno sviluppato una modalità di morte cellulare che mira ad annullare possibili effetti traumatici. Il termine apoptosi indica la morte cellulare che avviene tramite la realizzazione di cambiamenti morfologici sequenziali e specifici (Fig. 1).
L’apoptosi è oggi considerata solo una delle possibilità di eliminazione fisiologica delle cellule, mentre il meccanismo più generale a cui si fa riferimento per classificare la realizzazione di un programma genetico di morte cellulare è quello definito come PCD (Programmed Cell Death). Sono stati Lockshin e Williams nel 1965 ad affermare per primi che la morte delle cellule durante lo sviluppo di organismi pluricellulari avviene tramite l’attuazione di un programma ideato proprio per tale scopo. Il fenomeno fu definito appunto Programmed Cell Death, ovvero “morte cellulare programmata”. Nel 1972 Wyllie, Kerr e Currie hanno parlato di apoptosi, termine di origine greca utilizzato per descrivere la caduta dei petali dei fiori o quella delle foglie dagli alberi.
Tutte le cellule dell’organismo sono predisposte per attuare la PCD, che può essere invocata in tutte le fasi della vita di un organismo pluricellulare, sia durante lo sviluppo sia durante l’omeostasi dei tessuti nell’adulto. Eccone alcuni esempi:
- eliminazione di cellule ridondanti durante l’embriogenesi;
- rimodellamento dei tessuti durante la crescita;
- riparo e mantenimento dei tessuti;
- senescenza cellulare;
- modulazione del sistema immunitario;
- atrofia cellulare a seguito di mancanza di fattori di crescita;
- eliminazione di cellule con danni genetici
L’apoptosi si realizza attraverso una specifica sequenza di eventi biochimici che ha come scopo principale di arrecare il minimo danno al tessuto a cui appartiene la cellula che muore. Le molecole che prendono parte alla realizzazione del processo apoptotico si possono dividere in attivatori e inibitori dell’apoptosi.
Oggi si conoscono due vie per la sua realizzazione: la via estrinseca, regolata da segnali extracellulari, e la via intrinseca, regolata da segnali intracellulari. Le due vie non sono esclusive e spesso vengono attivate contemporaneamente, inoltre entrambe convergono verso l’attivazione dei medesimi enzimi effettori, le caspasi.
Le caspasi rappresentano un’ampia famiglia di enzimi proteolitici in grado di tagliare a livello di acido aspartico (di qui il nome) un gran numero di substrati. Ogni cellula degli organismi pluricellulari è predisposta a rispondere a un gran numero di segnali extracellulari e intracellulari, tra cui quelli che ne determinano la sopravvivenza. In condizioni normali è proprio il bilancio tra segnali di sopravvivenza e di suicidio a determinare il destino della cellula.
Al contrario delle caspasi, negli ultimi anni sono state scoperte proteine il cui ruolo principale è quello di costituire dei freni alla trasduzione del segnale apoptotico. Molti di tali inibitori sono statti individuati perché espressi dai virus come omologhi funzionali, col compito di impedire la morte della cellula ospite. In questo caso si tratta di segnali intracelluari che permettono al virus di replicarsi prima di provocare la lisi cellulare.
Lo studio di queste proteine ha permesso di individuare i fattori di crescita (growth factors), proteine extracellulari capaci di stimolare la proliferazione, il differenziamento cellulare e di prevenire l’apoptosi: sono tipiche molecole segnale usate per la comunicazione tra le cellule di un organismo, come le citochine (molecole infiammatorie) o ormoni che si legano a specifici recettori sulla membrana cellulare dei loro target.
La funzione principale dei fattori di crescita è il controllo esterno del ciclo cellulare, mediante l’abbandono della quiescenza cellulare (Fase G0) e l’entrata della cellula in fase G1 (di crescita).
Ma questa non è la loro unica funzione: i fattori di crescita, infatti, regolano l’entrata in mitosi, la sopravvivenza cellulare, la migrazione e il differenziamento cellulari. Insieme alla proliferazione cellulare essi promuovono sempre contemporaneamente il differenziamento cellulare, generando gli effetti più disparati a seconda del singolo fattore di crescita: ad esempio la proteina morfogenetica dell’osso (BPM) stimola il differenziamento degli osteoblasti, mentre il fattore di crescita dell’endotelio vascolare (VEGF) stimola la crescita dei vasi.
I termini “fattore di crescita” e “citochina” vengono spesso usati indifferentemente. Storicamente le citochine erano associate alle cellule ematopoietiche e immunologiche (per esempio linfociti e cellule della milza, timo e linfonodi). Per le cellule del sangue del midollo osseo, in cui le cellule si trovano in sospensione e non in un tessuto solido, è doveroso comunicare attraverso molecole solubili: diventò quindi chiaro che le stesse proteine utilizzate per i segnali delle cellule ematopoietiche e immunologiche erano usate da tutte le cellule e i tessuti dell’organismo in sviluppo. Oggi tuttavia si è soliti indicare come fattore di crescita una molecola che ha effetti positivi sulla divisione cellulare, mentre le citochine hanno un effetto neutro sulla proliferazione; ossia alcune citochine, come G-CSF e GM-CSF, hanno gli effetti di un fattore di crescita, mentre altre hanno un effetto inibente sulla proliferazione cellulare o addirittura inducono l’apoptosi.
I singoli fattori di crescita tendono a raggrupparsi in larghe famiglie di proteine strutturalmente simili. Sono famose le famiglie dei fattori di crescita insulino-simili (IGF), la BPM proteina morfogenetica dell’osso, le neurotrofine (NGF), il fattore di crescita dei fibroblasti (FGF). In pratica ogni tessuto ha il suo specifico fattore di crescita.
Negli ultimi anni è incrementato, grazie alle migliori conoscenze sulle strutture proteiche dei fattori di crescita, l’impiego di matrici proteiche fermentate di origine vegetale (concentrato proteico di patata o di soia) in grado di fornire per via alimentari i precursori dei growth factors. L’impiego di questi prodotti permette di ridurre la mortalità e incrementare l’indice di conversione attraverso una corretta stimolazione del sistema immunitario, un’inibizione dell’apoptosi e una riduzione del processo infiammatorio.









